AlphaFold2原理:注意力机制取代卷积网络,预测准确性提升超30%
本文经AI新媒体量子位(公众号ID:QbitAI)授权转载,转载请联系出处。
最近,DeepMind开源AlphaFold2,让学术圈再一次沸腾了。
这意味着,对于普通研究人员而言曾需要花几年时间才能破解的蛋白质结构,现在用AlphaFold2几小时就能算出来了!
那么,如此厉害的AlphaFold2究竟如何做到的呢?
DeepMind团队已经将它的详细信息在《Nature》上公开发表。

现在,就让我们来看看AlphaFold2的魔法是怎么实现的吧。
卷积消失了,Attention来了
论文中,研究人员强调AlphaFold2是一个完全不同于AlphaFold的新模型。
的确,它们使用的模型框架都不一样,这也是AlphaFold2准确性能够突飞猛进的主要原因。
此前AlphaFold中所有的卷积神经网络,现在都被替换成了Attention。
为什么要这样做呢?
我们首先要了解一下AlphaFold的工作原理:
它主要是通过预测蛋白质中每对氨基酸之间的距离分布,以及连接它们的化学键之间的角度,然后将所有氨基酸对的测量结果汇总成2D的距离直方图。
然后让卷积神经网络对这些图片进行学习,从而构建出蛋白质的3D结构。
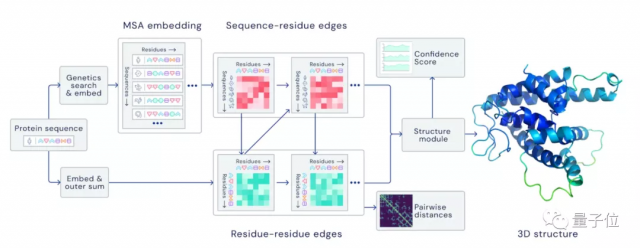
△AlphaFold主要架构
但这是一种从局部开始进行预测的方式,很有可能会忽略蛋白质结构信息的长距离依赖性。
而Attention的特点刚好可以弥补这一缺陷,它是一种模仿人类注意力的网络架构,可以同时聚焦多个细节部分。
这样可以使得框架预测的结果更加全面、准确。
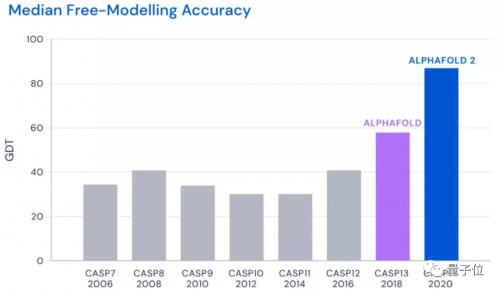
在CASP13中,AlphaFold预测的准确性还只有不到60分。
但是在CASP14中AlphaFold2就将准确性直接拔高到了92.4/100。
图网络+Attention
具体来看,AlphaFold2主要利用多序列比对(MSA),把蛋白质的结构和生物信息整合到了深度学习算法中。
它主要包括两个部分:神经网络EvoFormer和结构模块(Structure module)。
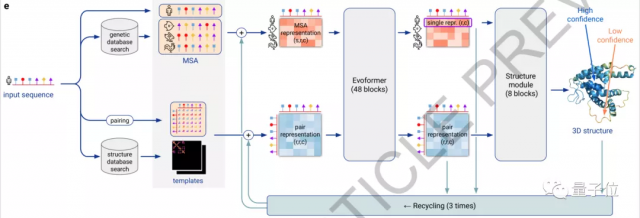
在EvoFormer中,主要是将图网络 (Graph networks)和多序列比对 (MSA)结合完成结构预测。
图网络可以很好表示事物之间的相关性,在这里,它可以将蛋白质的相关信息构建出一个图表,以此表示不同氨基酸之间的距离。
研究人员用Attention机制构建出一个特殊的“三重自注意力机制(Triangular self-attention)”,来处理计算氨基酸之间的关系图。
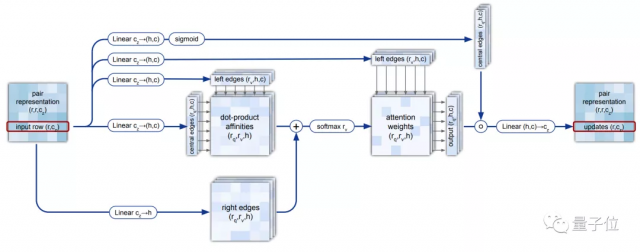
△三重自注意力机制(Triangular self-attention)
然后,他们将这一步得到的信息与多序列比对结合。
多序列比对主要是使相同残基的位点位于同一列,暴露出不同序列之间的相似部分,从而推断出不同蛋白质在结构和功能上的相似关系。
计算出的氨基酸关系与MSA进行信息交换,能直接推理出空间和进化关系的配对表征。
预测所有原子的3D结构
架构的第二部分是一个结构模块 (Structure Module),它的主要工作是将EvoFormer得到的信息转换为蛋白质的3D结构。
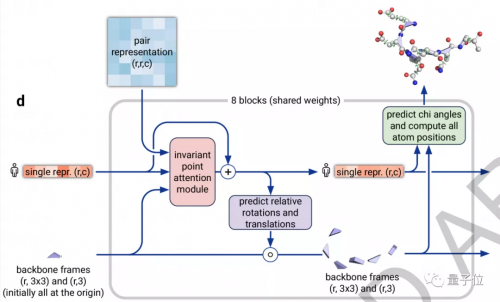
△结构模块(Structure module)
在这里,研究人员同样使用了Attention机制,它可以单独计算蛋白质的各个部分,称为“不变点注意力(invariant point attention)”机制。
它以某个原子为原点,构建出一个3D参考场,根据预测信息进行旋转和平移,得到一个结构框架。
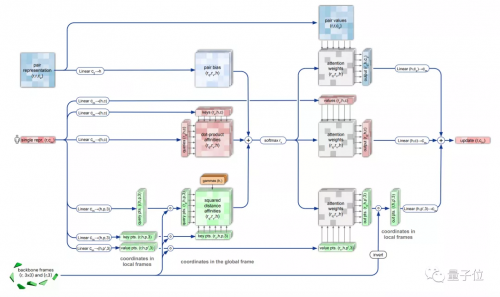
△不变点注意力(invariant point attention)
然后Attention机制会对所有原子都进行预测,最终汇总得出一个高度准确的蛋白质结构。
此外,研究人员还强调AlphaFold2是一个“端到端”的神经网络。
他们会反复把最终损失应用于输出结果,然后再对输出结果进行递归,不断逼近正确结果。
这样做既能减少额外的训练,还能大幅提高预测结构的准确性。
为破解蛋白质折叠谜题带来希望
Alphafold2的出现,能更好地预判蛋白质与分子结合的概率,从而极大地加速新药研发的效率。
此次Alphafold2开源,将进一步推动科学界前进。
据了解,目前DeepMind已经与瑞士的一些研究团队合作,通过预测蛋白质结构开展药物方面的研究。
事实上,研究Alphafold2预测程序本身,也为探索蛋白质结构折叠原理带来了希望。
芝加哥大学的计算生物学家Jinbo Xu就表示:
这些工具的开源,意味着科学界能够在此基础上开发出更加强大的软件。
论文地址:https://www.nature.com/articles/s41586-021-03819-2_reference.pdf
补充材料:https://static-content.springer.com/esm/art%3A10.1038%2Fs41586-021-03819-2/MediaObjects/41586_2021_3819_MOESM1_ESM.pdf*
相关阅读
-

云安全日报210527:Ubuntu配套LZ4解压缩软件发现执行任意代码漏洞,需要尽快升级
Ubuntu是一个以桌面应用为主的Linux操作系统。它是一个开放源代码的自由软件,提供了一个健壮、功能丰富的计算环境,既适合家庭使用又适用于商业环境。Ubuntu将为全球数百个公司提供商业支持。 ...
查看全文 -

云计算核心技术Docker教程:清理未使用的Docker对象
Docker采取了一种保守的方法来清理未使用的对象(通常称为“垃圾收集”),例如图像,容器,卷和网络:除非您明确要求Docker这样做,否则通常不会删除这些对象。这可能会导致Docker使用额外的磁盘空...
查看全文 -

消息称亚马逊、微软、谷歌正竞购波音公司10亿美元云合同
新浪科技讯 北京时间5月27日晚间消息,据报道,四位知情人士今日透露,亚马逊、微软和谷歌这三大云计算服务提供商,正在竞争波音公司(Boeing)价值10亿美元的云服务合同。 这些...
查看全文 -

亚马逊难逃反垄断惩罚?美国又有三个州加入调查
新浪科技讯 北京时间5月27日晚间消息,据报道,多位知情人士今日称,继加州、纽约州和华盛顿州之后,马萨诸塞州和宾夕法尼亚州的总检察长也加入到对亚马逊的反垄断调查中。 如今,越来越...
查看全文
您好!请登录